KRAS突变胰腺癌的铁死亡抵抗机制:HIF-2的双重防御通路解析
胰腺癌被冠以“癌王”之名,核心症结在于其对铁死亡疗法的天然抗性。一般逻辑认为,携带KRAS突变的肿瘤应更易受铁死亡影响,现实却截然相反。
研究背景与技术路径
《分子细胞》最新研究揭示了胰腺导管腺癌抵抗铁死亡的双重协同机制。研究团队采用缺氧环境与肿瘤间质液联合暴露的体外模型,系统筛选调控因子,最终锁定HIF-2为关键分子。
实验数据显示,单独缺氧或单独间质液处理对细胞保护效应微弱;两者联合时,保护作用呈指数级增强。这一结果暗示胰腺癌细胞在复杂的肿瘤微环境中整合多重生存信号。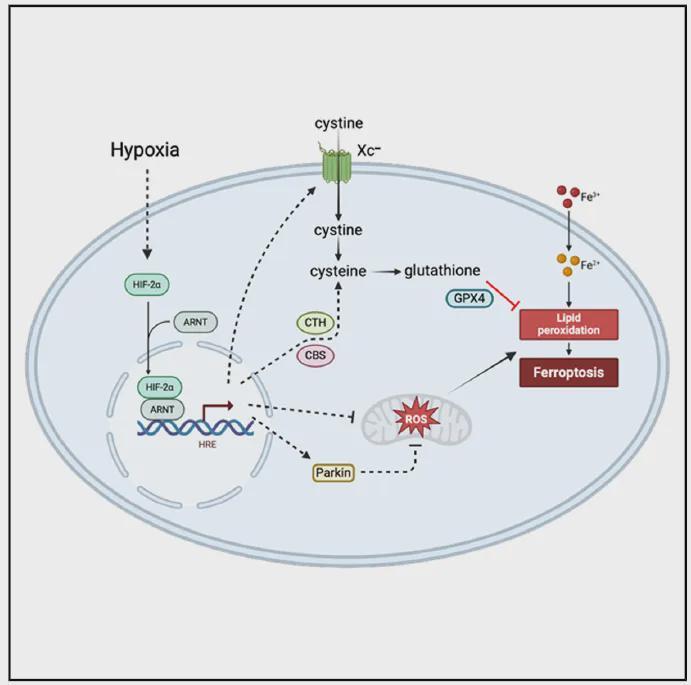
肿瘤低氧微环境的形成机制
胰腺肿瘤内部氧分压显著低于正常组织。病理机制涉及三个层面:肿瘤细胞高速增殖导致氧耗量激增;血管生成速率滞后于生长需求;纤维化基质形成物理屏障阻碍血氧扩散。三因素叠加造成氧供断崖式下跌。
低氧胁迫激活经典适应通路,HIF家族成员在此过程中扮演核心调控角色。但研究发现,HIF-2而非HIF-1在此特定场景下起决定性作用,暗示不同亚型在肿瘤微环境适应中分工明确。
HIF-2的双重防御通路
机制解析表明,HIF-2通过两条平行路径构建铁死亡抵抗屏障。通路一涉及谷胱甘肽代谢通路上调,提升细胞抗氧化容量,直接清除铁死亡执行过程中产生的脂质过氧化物;通路二通过增强自噬活性促进线粒体选择性降解,降低线粒体数量与呼吸功能,从源头削减活性氧产生速率。
两条通路协同运作形成闭环:抗氧化能力增强与氧化压力源头控制相互强化。抑制HIF-2表达后,上述保护效应完全消失,细胞恢复对铁死亡诱导剂的高度敏感性。
临床转化价值与靶点验证
研究结论直接指向HIF-2作为治疗靶点的可行性。通过药理学手段抑制HIF-2活性,可同时解除双重防御通路,恢复胰腺癌细胞对铁死亡疗法的响应能力。该策略有望突破当前治疗瓶颈,为约占全体胰腺癌85%的KRAS突变亚型提供新的干预路径。
